 | Rappeler les dťfinitions usuelles des acides et des bases. |
 | Rappeler que: H+,Cl-, Na+sont
hydratťs. On peut considťrer que H+est fixť ŗ
une molťcule d'eau pour donner H3O+et que H3O+est
entourť de molťcules d'eau. |
 | La dťfinition de BrŲnsted permet d'introduire les couples acide-base analogues aux
couples rťdox. |
 | Un acide est une entitť chimique (neutre ou chargťe) capable de donner un proton. |
 | Une base est une entitť chimique (neutre ou chargťe) capable de capter un proton.
Exemple:
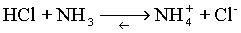
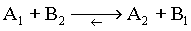
On voit qu'une rťaction acide-base est une rťaction de transfert de protons
sans transfert d'ťlectrons. |
 | La rťaction d'ionisation de l'eau:
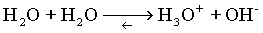
permet d'introduire les deux couples de l'eau. |