Classification
des acides et des bases |
||||||||
| La valeur des constantes d'équilibre des deux réactions: | ||||||||
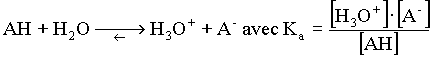 |
||||||||
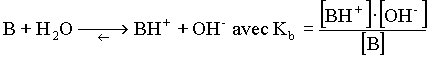 |
||||||||
permet de séparer les acides(ou les bases)en trois classes: *Forts Ka (ou Kb) trčs grand: Réaction pratiquement totale. *Faibles Ka (ou Kb) moyen: Réaction moyennement limitée. *Indifférents Ka (ou Kb) trčs petit: Réaction nulle. On montrera que pour un męme couple Ka.Kb=Ke. Pour pouvoir comparer tous les couples acide-base entre eux il est commode de les comparer ŕ un męme couple pris pour référence, le couple: H3O+/H2O. |
||||||||
L'élčve sera capable de(d'):
|